1. Der letzte Arbeitsfortschritt:
Zulassungserklärung für natürliches Paclitaxel:
● China CDE:
Am 13. Dezember 2021 wurde der CDE-Zusatzantrag abgeschlossen (der aktuelle CDE-Status ist im Bild dargestellt).und Hande akzeptierten vom 18. bis 20. Januar 2022 die GMP-Vor-Ort-Compliance-Inspektion der Lebensmittel- und Arzneimittelbehörde der Provinz Yunnan. Da CDE keine Genehmigungsdokumente mehr für die API-Registrierung und Änderungsprüfung ausstellen wird, wird es auch keine unterstützenden Dokumente dafür ausstellen vorläufig, kann aber bereits durch Präparate und Geräte referenziert werden.Entsprechend der Genehmigung von CDE finden Sie in der Änderungsbenachrichtigungs-E-Mail Informationen zu zugehörigen Prozess- und Standardänderungen..
Nach der Inspektion vor Ort wird Yunnan Hande den kommerziellen Verkauf auf dem chinesischen Markt offiziell wieder aufnehmen.Ihr Unternehmen kann die Produkte von Hande je nach Bedarf für Forschung und Entwicklung, kleine Tests, Pilottests und den klinischen Einsatz nutzen.Bewerbungsunterlagen können Hande CDE-Materialien direkt zitieren.
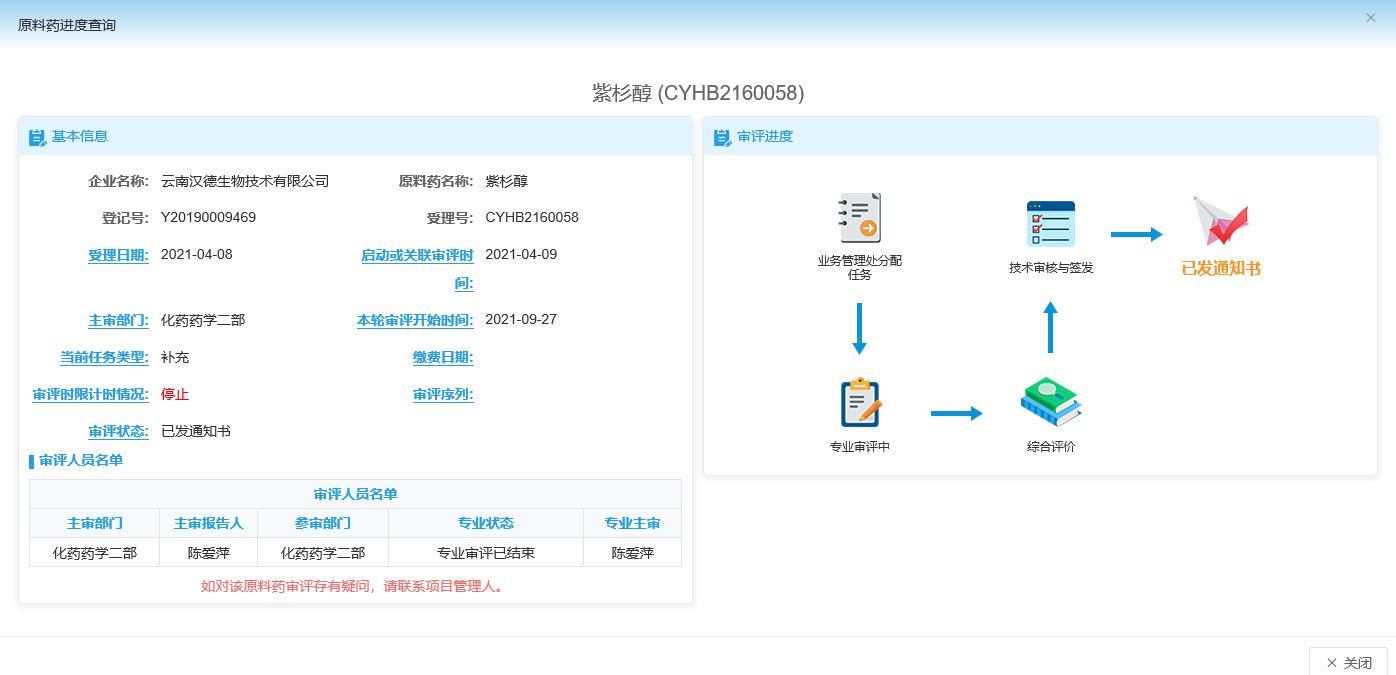
● EU EDQM:
Hande hat das CEP-Zertifikat und das „Zertifikatsdokument für den Export von APIs in die EU“ („WC“) erhalten und der EU-Markt hat den offiziellen kommerziellen Verkauf wieder aufgenommen.Wenn Ihr Unternehmen ein CEP-Zertifikat und ein Autorisierungsschreiben oder Produkte benötigt, kontaktieren Sie uns bitte rechtzeitig.
● US-amerikanische FDA:
Die DMF-Änderungsinformationen wurden übermittelt.
● Andere Länder oder Regionen:
Russland: Bestehende Kunden haben mit der Aktivierung der Registrierung begonnen;
Indien: DMF-Daten übermittelt;
Brasilien: DMF-Datenaufbereitung;
Japan: Registrierungsunterlagen wurden eingereicht;
Australisches TGA: In Vorbereitung;
EU GMP: in Vorbereitung;
Die übrigen Länder werden sich gleichzeitig bewerben.Zukünftig wird Hande Ihr Unternehmen dabei unterstützen, den internationalen strategischen Markt auszubauen.
2. Produktionslinie für halbsynthetisches 10-DAB-Paclitaxel:
Die Pilotproduktion ist beendet und die Tests sind abgeschlossen.Führen Sie jetzt Qualitätsuntersuchungen und Stabilitätsprüfungen durch.Der 3-Chargen-Verifizierungs-Batch-Produktionsplan beginnt im Januar 2022, nachdem die Installation und Inbetriebnahme der Ausrüstung abgeschlossen ist.
Regulatorischer Registrierungsplan für halbsynthetisches 10-DAB-Paclitaxel:
● China CDE: Dokument-Nr.: Y20210000685, der Start der Anwendung ist für das zweite Quartal 2022 geplant;
● EDQM und FDA: Planen Sie die Einreichung im vierten Quartal 2022.
3. Primäre Verarbeitungslinie:
Durch Statistiken vor Ort und Stichprobenprüfung mehrerer Eiben-Anpflanzungsgrundlagen wurde der jährliche Beschaffungsplan mit drei großen Pflanzgrundlagen umgesetzt, um eine ausreichende Rohstoffversorgung mit einer wirksamen Menge Paclitaxel sicherzustellen.Die jährliche Produktion von 10-DAB beträgt 2000 kg/Jahr, bei stabiler Qualität und langfristiger Versorgung.
● 10-DAB III-Regulierungsantrag:
DMF: Die DMF-Nummer wurde ermittelt.
2. Sonstige Informationen
1. Hande ist von der Epidemie betroffen und wird nicht mehr an der CPHI-Ausstellung teilnehmen.Um Ihr Unternehmen besser bedienen zu können, werden wir weiterhin Kundenbesuche durchführen und mit besseren Dienstleistungen bei der Marktentwicklung Ihres Unternehmens zusammenarbeiten.
Zeitpunkt der Veröffentlichung: 18. Februar 2022